Filtrowanie pytań
Jaką objętość roztworu NaOH o stężeniu 1 mol/dm3 należy użyć, aby przygotować 50 cm3 roztworu NaOH o stężeniu 0,4 mol/dm3?
Ropa naftowa stanowi mieszankę węglowodorów. Jaką metodę wykorzystuje się do jej rozdzielania na składniki?
W mikrobiologicznych badaniach, dezynfekcja ma na celu eliminację
Który z etapów przygotowania próbek do analizy opisano w ramce?
| Proces polegający na usuwaniu wody z zamrożonego materiału na drodze sublimacji lodu, tzn. bezpośredniego jego przejścia w stan pary z pominięciem stanu ciekłego. |
Substancje utleniające opisuje piktogram

Wskaź zestaw reagentów oraz przyrządów wymaganych do przygotowania 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3?
Jakie aspekty nie są objęte badaniami organoleptycznymi olejów rafinowanych?
Sporządzono 250 cm3 roztworu glicerolu o gęstości 1,05 g/cm3 w temperaturze 20°C. Korzystając z danych zamieszczonych w tabeli, określ stężenie procentowe sporządzonego roztworu glicerolu.
| Glicerolu [%] | 10% | 20% | 30% | 50% |
|---|---|---|---|---|
| d20 [g/dm3] | 1023,70 | 1048,40 | 1073,95 | 1127,20 |
Aby przygotować oznaczenia spektrofotometryczne kwasu acetylosalicylowego w zakresie nadfioletu, należy sporządzić cztery wzorce o objętości 50 cm3 każdy. Wzorce te powinny być stworzone poprzez odważenie kwasu salicylowego z dokładnością do 0,0001 g oraz rozpuszczenie odważonych ilości w 0,1000 mol/dm3 roztworze NaOH. Jaki sprzęt oraz w jakiej ilości, oprócz wagi analitycznej i łyżeczki, trzeba użyć do przygotowania tych wzorców?
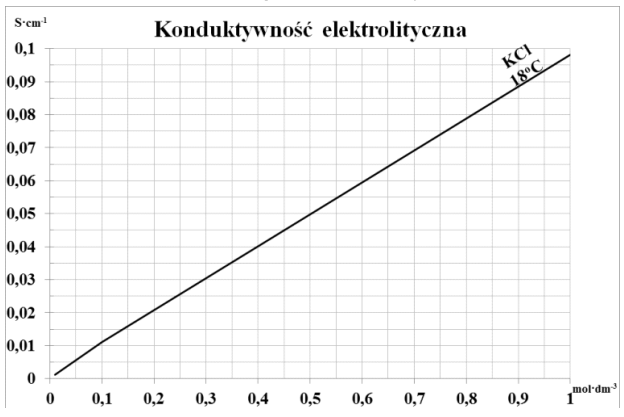
W celu wyznaczenia stężenia badanej próbki chlorku potasu, wykonano krzywą wzorcową zależności konduktywności elektrolitycznej od stężenia. Przewodność badanego roztworu wyniosła 0,045 S∙cm-1. Stężenie badanego roztworu KCl wynosi
Roztwory o ściśle określonym stężeniu, używane w analizach miareczkowych, nazywamy
W metodzie analitycznej zapisano. Który parametr metody analitycznej opisano w ramce?
| Różnica w otrzymanych wynikach dwóch oznaczeń wykonanych równocześnie lub w krótkim przedziale czasu na tej samej próbce, przez tego samego analityka, w takich samych warunkach, nie może przekraczać 1,5 g na 100 g oznaczanej próbki. |
Proces mineralizacji próbki, który polega na jej spopieleniu w piecu muflowym w temperaturze 300-500°C i rozpuszczeniu pozostałych resztek w kwasach w celu oznaczenia zawartości metali ciężkich, to mineralizacja
Na schemacie przedstawiono mechanizm działania wskaźników
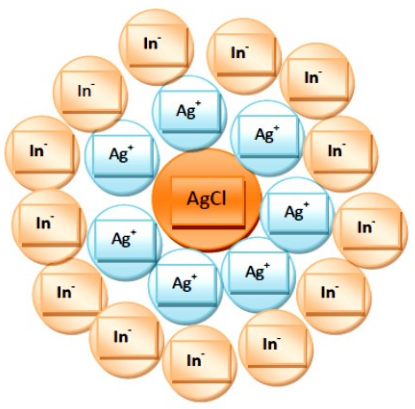
Zjawisko, w którym obce jony są mechanicznie zatrzymywane przez szybko rosnący kryształ, określane jest mianem
Etykieta roztworu kwasu azotowego(V) o koncentracji 6 mol/dm3 powinna zawierać nazwę substancji oraz
Deminimalizowaną wodę można uzyskać przez
Do barwienia preparatów metodą Grama w badaniach mikrobiologicznych używa się płynu Lugola, który jest
Na podstawie danych zawartych w tabeli, wskaż zestaw substancji uporządkowanych według rosnącej temperatury topnienia.
| Substancja | pirydyna | benzen | etanol |
|---|---|---|---|
| Temperatura wrzenia [°C] | 115,5 | 80,1 | 78,3 |
| Temperatura topnienia [°C] | -41,6 | 5,5 | -114,1 |
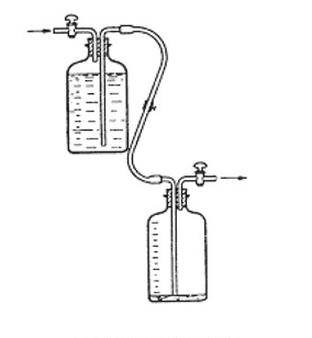
Który proces przedstawiono na zamieszczonym rysunku?
Podczas ilościowego oznaczania zawartości chlorków w próbce wody zachodzą przemiany przedstawione równaniami reakcji: Wskaż typ reakcji, do którego należą.
| Ag+ + Cl- → AgCl |
| 2 Ag+ + CrO42- → Ag2CrO4 |
W dwóch niezidentyfikowanych probówkach znajdują się roztwory: w jednej - glukozy, a w drugiej - sacharozy. Jakiego odczynnika należy użyć, aby rozpoznać glukozę?
Jakie jest stężenie roztworu HNO3, który powstał w wyniku połączenia 50 cm3 roztworu HNO3 o stężeniu 0,2 mol/dm3 oraz 25 cm3 roztworu HNO3 o stężeniu 0,5 mol/dm3?
Na ilustracji przedstawiono

Bufor amonowy to system kwasowo-zasadowy złożony z wodnego roztworu
Instrukcja dotycząca przygotowania wzorcowego roztworu NaCl
0,8242 g NaCl, które wcześniej wysuszono w temperaturze 140 °C do stałej masy, należy rozpuścić w kolbie miarowej o pojemności 1 dm3 w wodzie podwójnie destylowanej, a następnie uzupełnić do kreski tym samym rodzajem wody.
Z treści instrukcji wynika, że odpowiednio skompletowany sprzęt wymagany do sporządzenia wzorcowego roztworu NaCl, oprócz naczynia wagowego, powinien zawierać
Konduktometria to technika analityczna, która opiera się na pomiarze
Która część małej partii materiału jest najczęściej pobierana w celu przygotowania próbki ogólnej?
Określ wartość opałową (Qi) węgla kamiennego, którego ciepło spalania jest równe 18752 J/g, zawartość popiołu wynosi 8,7%, zawartość wilgoci wynosi 4,1%.
| Qi = Qsp - 24,42 · (W + 8,94 · ZH) |
Qsp – ciepło spalania, J/g W – zawartość wilgoci, % 24,42 – ciepło parowania wody w temp. 25°C odpowiadające 1% wody w paliwie, J/g 8,94 – współczynnik przeliczenia wodoru na wodę, % ZH – zawartość wodoru w próbce paliwa, % Zawartość wodoru w próbce należy obliczyć z dokładnością do części dziesiątych ze wzoru: ZH = (100 - W - A) / 18,5 A – zawartość popiołu, % |
Do wykrywania pierwiastków w niskich stężeniach w badaniach spektrograficznych należy używać reagentów
Rozpuszczalnik stosowany w procesie krystalizacji powinien
Skręcalność optyczną cukrów mierzy się przy użyciu
Na rysunku przedstawiono
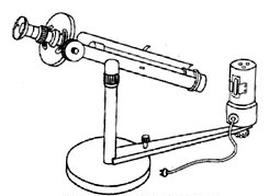
Na rysunku przedstawiono
Aby przygotować roztwór wzorcowy potrzebny do oznaczania miana, konieczne jest użycie odczynnika chemicznego o czystości przynajmniej
Do systemu odprowadzania ścieków, w formie rozcieńczonego roztworu wodnego o maksymalnej masie 100 g na raz, można wprowadzić
Na podstawie informacji zawartych w tabeli wskaż, który adsorbent należy zastosować podczas oznaczania karotenów.
| Podział adsorbentów według zastosowania | |
|---|---|
| Adsorbent | Przykłady zastosowania |
| Tlenek glinu zasadowy | aminy, węglowodory, alkaloidy, zasady heterocykliczne |
| Tlenek glinu obojętny | aminy, amidy, alkaloidy, glikozydy |
| Tlenek glinu kwasowy | barwniki, związki kwasowe |
| Żel krzemionkowy | aminy, kwasy karboksylowe, amidy, węglowodory, inne związki obojętne |