Filtrowanie pytań
Przygotowywanie sprzętu, odcz…
A. Czysty
B. Czystość do analizy
C. Czystość chemiczna
D. Czystość spektralna
Wykonywanie badań analityczny…
Głównym elementem określonego stopu jest miedź, a dodatkowymi składnikami są ołów oraz cynk. Po rozpuszczeniu tego stopu w kwasie azotowym(V) w jaki sposób należy oznaczyć zawartość miedzi?
A. metodą refraktometryczną
B. metodą elektrolityczną
C. mierząc przewodnictwo roztworu
D. metodą wagową
Przygotowywanie sprzętu, odcz…
Jaką objętość powinna mieć kolba miarowa, aby przygotować mianowany roztwór NaOH o stężeniu 0,050 M z analitycznej odważki, która zawiera 0,1 mola NaOH?
A. 1 dm3
B. 2 dm3
C. 200 cm3
D. 100 cm3
Wykonywanie badań analityczny…
W dwóch nieoznakowanych kolbach znajdują się roztwory HCl o różnych stężeniach: 0,1 mol/dm3 oraz 0,01 mol/dm3. Aby odróżnić te roztwory, nie można zastosować
A. papierków lakmusowych
B. miareczkowania konduktometrycznego przy użyciu mianowanego roztworu NaOH
C. miareczkowania alkacymetrycznego przy użyciu mianowanego roztworu NaOH z oranżem metylowym
D. pomiaru pH korzystając z pH-metru oraz skalibrowanej elektrody szklanej
Wykonywanie badań analityczny…
Wskaźnik zanieczyszczenia wody bakterią jelitową - miano coli równe 10 - oznacza, że
A. w 10 cm3 wody znajduje się co najmniej 1 bakteria Escherichia coli
B. w 10 dm3 wody znajduje się co najmniej 1 bakteria Escherichia coli
C. w 1 dm3 wody występuje 10 bakterii z rodzaju Escherichia coli
D. w 1 cm3 wody znajduje się 10 bakterii z rodzaju Escherichia coli
Wykonywanie badań analityczny…
Urządzeniem używanym do hodowli bakterii w środowisku beztlenowym jest
A. autoklaw
B. pasteryzator
C. anaerostat
D. boks laminarny
Przygotowywanie sprzętu, odcz…
Jak przebiega procedura unieszkodliwiania rozlanego kwasu siarkowego(VI)?
A. zbieraniu kwasu tlenkiem wapnia w celu późniejszej utylizacji
B. dokładnym spłukaniu miejsc z kwasem roztworem wodorotlenku sodu
C. spłukaniu miejsc z kwasem gorącą wodą
D. dokładnym spłukaniu miejsc z kwasem roztworem węglanu sodu
Wykonywanie badań analityczny…
Zabarwienie roztworu soli prostej w wodzie na zielono wskazuje na obecność jonu
A. Ni2+
B. Mn2+
C. Co2+
D. Cu2+
Wykonywanie badań analityczny…
Na podstawie informacji zamieszczonych w tabeli wskaż, do którego rodzaju nawozów azotowych należy saletra potasowa.
| Podział nawozów azotowych | Średnia zawartość azotu [%] | MN = 14 g/mol MO = 16 g/mol MK = 39 g/mol | |
|---|---|---|---|
| I. | saletrzane | 15 | |
| II. | amonowe | 25 | |
| III. | saletrzano-amonowe | 34 | |
| IV. | amidowe | 46 |
A. IV.
B. II.
C. I.
D. III.
Wykonywanie badań analityczny…
Na rysunku przedstawiono wykonanie analizy metodą
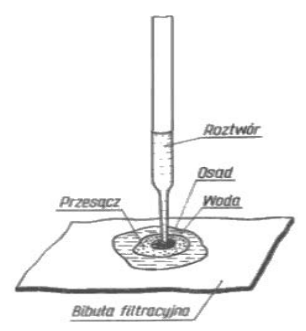
A. jakościowej analizy kroplowej.
B. chromatografii cieczowej.
C. ilościowej analizy kroplowej.
D. chromatografii cienkowarstwowej.
Wykonywanie badań analityczny…
Elektroforeza to technika wykorzystywana głównie do segregacji mieszaniny
A. alkoholi
B. węglowodanów
C. tłuszczów
D. białek
Wykonywanie badań analityczny…
W celu oceny jakości masła wykonano oznaczenie liczby kwasowej LK, liczby zmydlania LZ i liczby nadtlenkowej LOO. Wyniki zapisano w tabeli.
Wartość liczby estrowej LE w badanym maśle wynosi
| Liczba | Wartość zmierzona |
|---|---|
| LZ | 196,8 mg KOH/1g |
| LK | 1,2 mg KOH/1g |
| LE | ? |
| LOO | 4,25 milirównoważnika aktywnego tlenu/ kg |
A. 195,6 mg KOH/1g
B. 164,0 mg KOH/1g
C. 198,0 mg KOH/1g
D. 234,7 mg KOH/1g
Wykonywanie badań analityczny…
W trakcie analizy przeprowadzonej metodą fotometrii płomieniowej próbkę nawozu o wadze 0,1000 g rozpuszczono w 250 cm3 wody destylowanej. Po wykonaniu badań uzyskano zawartość potasu równą 0,0830 mg/cm3. Jaką wartość procentową K2O ma badany nawóz i czy mieści się ona w normie, jeśli współczynnik przeliczeniowy K na K2O wynosi 1,205, a zawartość procentowa K2O w nawozie powinna być w zakresie 40-50%?
A. 2,5% i nie jest zgodna z normą
B. 25% i nie jest zgodna z normą
C. 45% i jest zgodna z normą
D. 40% i jest zgodna z normą
Wykonywanie badań analityczny…
W trakcie mikrobiologicznych analiz żywności przed posiewem konieczne jest dokonanie rozcieńczenia próbki. W tym celu po dokładnym wymieszaniu badanego płynu pobiera się 10 cm3 za pomocą jałowej pipety, umieszcza w kolbie z 90 cm3 płynu rozcieńczającego i starannie miesza. Następnie z pierwszego rozcieńczenia przenosi się 1 cm3 do probówki, wzbogaconej o 9 cm3 płynu rozcieńczającego. W ten sposób uzyskuje się rozcieńczenie
A. 1:90
B. 1:9
C. 1:100
D. 1:10
Przygotowywanie sprzętu, odcz…
Podstawowy zestaw do filtracji, oprócz statywu i sączka, obejmuje
A. lejka, zlewki, 2 bagietek
B. lejka, 2 kolb stożkowych, bagietki
C. lejka, 2 zlewki, bagietki
D. lejka, kolby stożkowej, zlewki
Wykonywanie badań analityczny…
W tabeli przedstawiono charakterystykę
| Charakterystyka wybranych metod optycznych stosowanych w analizie instrumentalnej | ||
|---|---|---|
| Metoda | Obserwowane zjawisko | Pomiar |
| 1 | załamanie światła | współczynnik załamania światła padającego na powierzchnię próbki |
| 2 | skręcanie płaszczyzny światła spolaryzowanego | kąt skręcenia płaszczyzny polaryzacji światła |
| 3 | rozproszenie promieniowania | natężenie wiązki światła rozproszonego wychodzącego z kuwety pomiarowej |
A. 1 - refraktometrii, 2 - polarymetrii, 3 - nefelometrii.
B. 1 - polarymetrii, 2 - refraktometrii, 3 - nefelometrii.
C. 1 - refraktometrii, 2 - nefelometrii, 3 - polarymetrii.
D. 1 - nefelometrii, 2 - refraktometrii, 3 - polarymetrii.
Wykonywanie badań analityczny…
Przy pomocy polarymetru wykonuje się pomiar
A. transmitancji
B. kąta obrotu płaszczyzny światła spolaryzowanego
C. absorbancji
D. współczynnika załamania światła
Przygotowywanie sprzętu, odcz…
Korzystając z danych w tabeli wskaż, ile cm3 36% roztworu HCl należy użyć, aby przygotować 250 cm3 0,1-molowego roztworu tego kwasu.
| % wagowy [%] | d420 [g/cm3] | m HCl w 100 cm3 [g/100cm3] | CM HCl [mol/dm3] |
|---|---|---|---|
| 30 | 1,1492 | 34,48 | 9,46 |
| 32 | 1,1593 | 37,10 | 10,17 |
| 34 | 1,1691 | 39,75 | 10,90 |
| 36 | 1,1789 | 42,44 | 11,64 |
A. 2,52 cm3
B. 2,15 cm3
C. 2,13 cm3
D. 2,50 cm3
Wykonywanie badań analityczny…
Schematyczny rysunek ezy, przyrządu używanego w laboratoriach mikrobiologicznych, został oznaczony na rysunku cyfrą
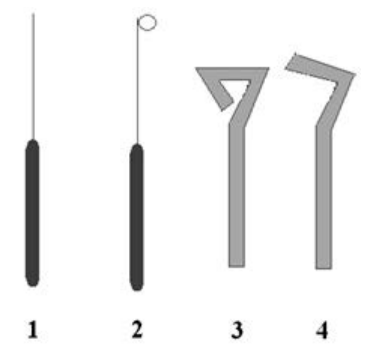
A. 3.
B. 1.
C. 2.
D. 4.
Wykonywanie badań analityczny…
Jaką wartość współmierności ma kolba miarowa o objętości 500 cm3 oraz pipeta jednomiarowa o objętości 20 cm3?
A. 25
B. 0,04
C. 50
D. 2,5
Wykonywanie badań analityczny…
W jakiej proporcji molowej EDTA reaguje z jonami Zn2+?
A. 1 : 3
B. 1 : 4
C. 1 : 2
D. 1 : 1
Wykonywanie badań analityczny…
Czynniki biologiczne, które są rozproszone w atmosferze, takie jak mikroorganizmy oraz fragmenty roślin i zwierząt, powiązane z drobnymi cząstkami stałymi (pyłem) lub kroplami cieczy, to
A. biofilm.
B. smog.
C. bioaerozol.
D. mikroflora.
Wykonywanie badań analityczny…
Wskaż błędnie określone efekty reakcji analitycznych kationów I grupy.
| Odczynnik strącający | Reakcje analityczne | |||
|---|---|---|---|---|
| Ag+ | Hg22+ | Pb2+ | ||
| A. | HCl | biały osad AgCl rozpuszczalny w NH3·H2O | biały osad Hg2Cl2 | biały osad PbCl2 rozpuszczalny w gorącej wodzie |
| B. | H2SO4 | biały Ag2SO4 (ze stężonych roztworów), rozpuszczalny w gorącej wodzie | biały osad Hg2SO4 rozpuszczalny w wodzie królewskiej | biały osad PbSO4 rozpuszczalny w roztworze NaOH |
| C. | NaOH | brunatny osad Ag2O rozpuszczalny w NH3·H2O | czarny osad HgO i Hg | biały osad Pb(OH)2 rozpuszczalny w roztworze NaOH |
| D. | NH3aq | brunatny jon kompleksowy Ag(NH3)2+ | biały osad soli amidortęciowej rozpuszczalny w stężonym HNO3 | żółty osad Pb(OH)2 rozpuszczalny w gorącej wodzie |
A. C.
B. D.
C. A.
D. B.
Przygotowywanie sprzętu, odcz…
Na rysunku przedstawiono proces
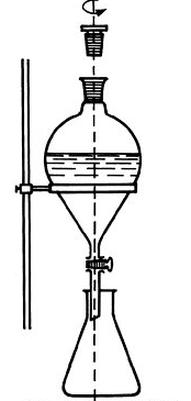
A. ekstrakcji.
B. sedymentacji.
C. sączenia.
D. destylacji.
Wykonywanie badań analityczny…
Na zmiareczkowanie 10 cm3 NaOH zużyto 2 cm3 0,1-molowego roztworu H2SO4. Ilość wodorotlenku sodu w badanej próbce w g/100 cm3 wynosi (Na — 23 g/mol, O — 16 g/mol, H — 1 g/mol)
A. 0,008 g/100 cm3
B. 0,16 g/100 cm3
C. 0,016 g/100 cm3
D. 0,0008 g/100 cm3
Wykonywanie badań analityczny…
Twardość całkowita wody
A. nazywana jest przemijającą, ponieważ znika podczas gotowania
B. definiuje ilość chlorków, siarczanów i azotanów, głównie wapnia i magnezu
C. odnosi się do całkowitej ilości wodorowęglanów wapnia i magnezu
D. dotyczy łącznej zawartości jonów wapnia i magnezu oraz innych jonów metali, które wpływają na twardość wody
Wykonywanie badań analityczny…
Do czego służy aparat Soxhleta w kontekście ekstrakcji składnika?
A. łatwego do ekstrahowania z fazy gazowej
B. trudnego do ekstrakcji z fazy ciekłej
C. łatwego do ekstrakcji z fazy ciekłej
D. trudnego do wyizolowania z fazy stałej
Przygotowywanie sprzętu, odcz…
Na rysunku przedstawiono wagę

A. mikroanalityczną.
B. automatyczną.
C. precyzyjną.
D. hydrostatyczną.
Przygotowywanie sprzętu, odcz…
Na etykiecie kwasu siarkowego(VI) znajduje się piktogram pokazany na rysunku. Oznacza to, że substancja ta jest
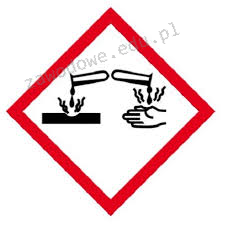
A. nieszkodliwa.
B. mutagenna.
C. rakotwórcza.
D. żrąca.
Wykonywanie badań analityczny…
W jakiej metodzie analizy instrumentalnej wykorzystuje się zdolność substancji optycznie aktywnej do skręcania płaszczyzny światła spolaryzowanego?
A. W turbidymetrii
B. W nefelometrii
C. W polarymetrii
D. W refraktometrii
Przygotowywanie sprzętu, odcz…
Etykieta roztworu kwasu azotowego(V) o koncentracji 6 mol/dm3 powinna zawierać nazwę substancji oraz
A. masę, datę przygotowania i numer katalogowy
B. koncentrację, ostrzeżenia H oraz datę przygotowania
C. koncentrację, producenta i wykaz zanieczyszczeń
D. masę, koncentrację i numer katalogowy
Przygotowywanie sprzętu, odcz…
Podczas pobierania skoncentrowanego roztworu kwasu solnego konieczne jest pracowanie w włączonym dygestorium oraz zastosowanie
A. fartucha, okularów ochronnych, maski ochronnej, rękawic lateksowych
B. rękawic odpornych na kwasy, maski ochronnej
C. okularów ochronnych, rękawic lateksowych, maski ochronnej
D. fartucha, okularów ochronnych, rękawic odpornych na kwasy
Wykonywanie badań analityczny…
Związki lotne, które występują w wielu roślinach i mogą być wydobywane, np. poprzez destylację z parą wodną lub dzięki ciągłej ekstrakcji w aparacie Soxhleta, to
A. glikozydy
B. alkaloidy
C. terpeny
D. flawonoidy
Wykonywanie badań analityczny…
Jakiego koloru płomień uzyskuje się dzięki sole miedzi?
A. ceglastoczerwony
B. karminowy
C. żółty
D. zielony
Wykonywanie badań analityczny…
Na diagramie słupkowym przedstawiono wyniki analizy sitowej surowca w formie proszkowej. W jakiej kolejności zamontowano sita w wytrząsarce, licząc je od naczynia zbierającego?
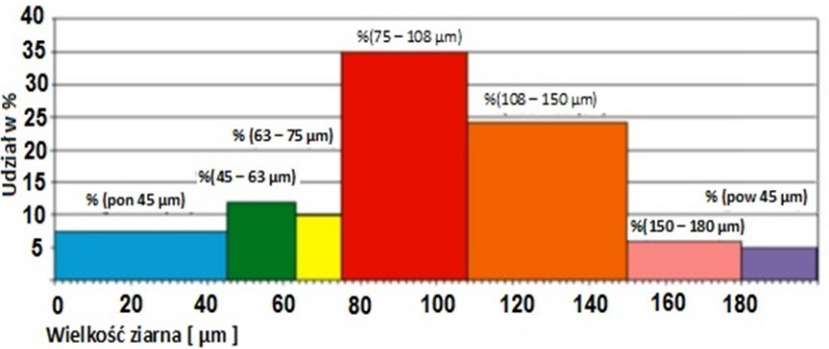
A. 75 µm, 108 µm, 150 µm, 180 µm 63 µm, 45 µm.
B. 45 µm, 63 µm, 75 µm, 108 µm, 150 µm, 180 µm.
C. 150 µm, 45 µm, 63 µm, 75 µm, 108 µm, 180 µm.
D. 180 µrn, 150 µrn, 108 µrn, 75 µrn, 63 µrn, 45 µrn.
Wykonywanie badań analityczny…
Analityczne mnożniki dla wagowego oznaczania wapnia (M = 40,08 g/mol) w formie CaC2O4 (M = 128,10 g/mol), CaCO3 (M = 100,09 g/mol) oraz CaO (M = 56,08 g/mol) wynoszą odpowiednio
A. 0,3128; 0,4378; 0,7147
B. 3,1961; 2,4972; 1,3992
C. 0,7147; 2,2842; 1,7992
D. 0,3129; 0,4004; 0,7147
Wykonywanie badań analityczny…
Na rysunku przedstawiono schemat procesu
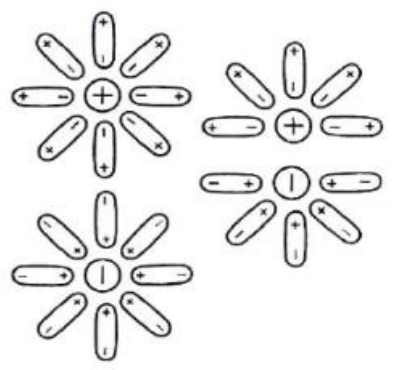
A. hydrolizy, polegającego na reakcji cząsteczek wody ze związkami obecnymi w wodzie.
B. okluzji, polegającego na wiązaniu jonów obcych w sieci krystalicznej substancji.
C. dyfuzji, polegającej na samorzutnym rozprzestrzenianiu się i przenikaniu cząsteczek w cieczy.
D. solwatacji, polegającego na oddziaływaniu rozpuszczalnika polarnego na rozpuszczaną substancję jonową.
Przygotowywanie sprzętu, odcz…
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
A. krystalizacją
B. sublimacją
C. dekantacją
D. ekstrakcją
Przygotowywanie sprzętu, odcz…
Na rysunku przedstawiono palnik Bunsena. Którym numerem oznaczono element do regulowania dopływu powietrza?

A. 4
B. 1
C. 2
D. 3
Wykonywanie badań analityczny…
Czym charakteryzuje się barwa roztworu zawierającego jony Cr2O72-?
A. zielona
B. żółta
C. pomarańczowa
D. niebieska