Wskaż, do jakiego typu należą zamieszczone równania reakcji.
| I. 2 Mg + O2 → 2 MgO |
| II. 2 KMnO4 → K2MnO4 + MnO2 + O2 |
| III. BaCl2 + H2SO4→ BaSO4 + 2 HCl |
| I. 2 Mg + O2 → 2 MgO |
| II. 2 KMnO4 → K2MnO4 + MnO2 + O2 |
| III. BaCl2 + H2SO4→ BaSO4 + 2 HCl |
| Do kolby stożkowej o pojemności 300 cm3 pobrać dokładnie 25 cm3 badanego mleka i rozcieńczyć wodą destylowaną do objętości 50 cm3. Dodać 2-3 krople fenoloftaleiny i miareczkować mianowanym roztworem wodorotlenku sodu do uzyskania lekko różowego zabarwienia. |
| I | II | III | IV | V |
|---|---|---|---|---|
| Ca(OH)2(aq) | NaOH(s) | HNO3(stęż) | CuO(s) | CaO(s) |
| Zawartość chlorowodoru w próbce można obliczyć wg wzoru: mB = CA · VA⁄1000 · pB⁄pA · MB w którym: mB – masa analizowanej substancji [g] CA – stężenie titranta [mol/dm3] VA – objętość titranta [cm3] pA i pB – współczynniki stechiometryczne reakcji, odpowiednio titranta i substancji oznaczanej MB – masa molowa substancji oznaczanej; 36,46 g/mol Do oznaczenia zużyto średnio 20,0 cm3 titranta, którego stężenie wynosiło 0,1000 mol/dm3. Obliczono masę próbki, która wyniosła 0,07292 g. |
| A. | HCl + NaOH → NaCl + H2O |
| B. | 3HCl + Al(OH)3 → AlCl3 + 3H2O |
| C. | 2HCl + Na2CO3 → 2NaCl + H2O + CO2 |
| D. | 2HCl + Na2B4O7 + 5H2O → 4H3BO3 + 2NaCl |
| Jeżeli w wodzie zostanie rozpuszczona α-D-glukopiranoza, to roztwór tuż po rozpuszczeniu wykazuje skręcalność właściwą [α]D= +112,2°, lecz w miarę upływu czasu skręcalność ta stopniowo spada do wartości charakterystycznej w stanie równowagi, mianowicie [α]D= +52,7° |
| Zmiany barw najważniejszych wskaźników kwasowo-zasadowych | ||||
|---|---|---|---|---|
| Wskaźnik | Barwa w środowisku | Zakres pH zmiany barwy | ||
| Kwasowym | Obojętnym | Zasadowym | ||
| oranż metylowy | czerwona | żółta | żółta | 3,2÷4,4 |
| lakmus (mieszanina substancji) | czerwona | fioletowa | niebieska | 4,5÷8,2 |
| fenoloftaleina | bezbarwna | bezbarwna | malinowa | 8,2÷10,0 |
| wskaźnik uniwersalny (mieszanina substancji) | czerwona (silnie kwaśne) pomarańczowa (słabo kwaśne) | żółta | niebieska (silnie zasadowe) zielona (słabo zasadowe) | co jeden stopień skali |
| herbata | żółta | czerwona-brunatna | brązowa | |
| sok z czerwonej kapusty | fioletowa | niebieska | zielona | |
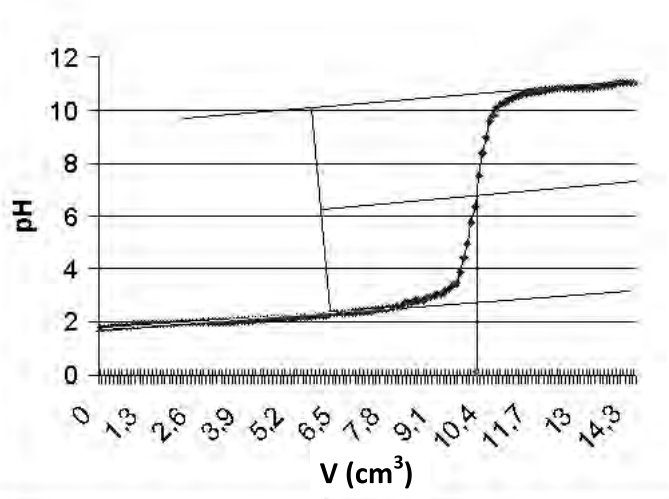
| Procedura oznaczania kwasowości wody metodą miareczkowania wobec wskaźników. |
|---|
| Do kolby stożkowej odmierzyć 100 cm3 badanej wody, dodać 3 krople oranżu metylowego i miareczkować roztworem NaOH o stężeniu 0,05 mol/dm3 do pierwszej zmiany barwy z różowej na słomkowożółtą. Następnie dodać 10 kropli fenoloftaleiny i miareczkować roztworem NaOH do wyraźnie różowego zabarwienia utrzymującego się przez 3 minuty. |
| mannoza | maltoza | mannoza | celuloza |
| glukoza | glukoza | glukoza | glukoza |
| sacharoza | fruktoza | fruktoza | ryboza |
| A | B | C | D |
| Więcej niż | Mniej niż | |
|---|---|---|
| A. | 0,20 μg/cm3 | 0,30 μg/cm3 |
| B. | 2 μg/cm3 | 3 μg/cm3 |
| C. | 20 μg/cm3 | 30 μg/cm3 |
| D. | 200 μg/cm3 | 300 μg/cm3 |
