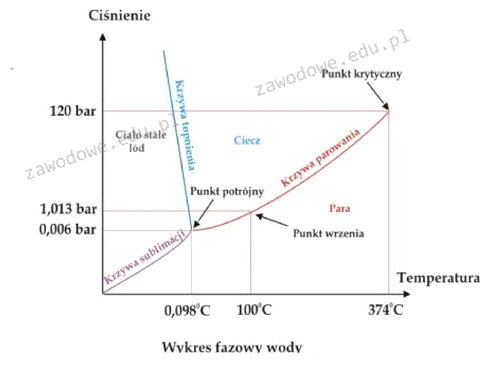
Odpowiedź Cieczy jest poprawna, ponieważ analizy wykresu fazowego wody w temperaturze 373K i ciśnieniu 100 barów jednoznacznie wskazują na stan ciekły. Woda w tym stanie znajduje się poniżej krzywej parowania, co oznacza, że nie osiągnęła jeszcze punktu wrzenia, który w standardowych warunkach wynosi 373K przy ciśnieniu atmosferycznym. W praktyce, stan ciekły wody jest kluczowy w wielu procesach przemysłowych, takich jak chłodzenie, transport chemikaliów oraz w różnych zastosowaniach w laboratoriach. Zrozumienie stanu skupienia wody w różnych warunkach ciśnienia i temperatury jest fundamentalne w inżynierii chemicznej, ponieważ wpływa na wydajność procesów reakcyjnych oraz transport cieczy. Wiedza ta jest również istotna w dziedzinie ochrony środowiska, gdzie kontrola stanu wody jest kluczowa dla oceny jakości wód oraz podejmowania działań w przypadku zagrożeń.
Wybór odpowiedzi związanych z ciałem stałym, parą lub sublimatem wynika często z nieporozumień dotyczących stanów skupienia materii i ich zachowania w różnych warunkach. Ciało stałe woda może przyjąć tylko w temperaturach poniżej 273K przy ciśnieniu atmosferycznym, co sprawia, że woda nie może być w stanie stałym przy 373K. Para wodna z kolei to stan, w którym cząsteczki wody mają wystarczającą energię, aby przekształcić się w gaz, co nie ma miejsca w podanych warunkach. Sublimacja, czyli przejście ze stanu stałego bezpośrednio w gaz, dotyczy głównie substancji takich jak lód, ale woda w stanie ciekłym nie podlega tej transformacji do 373K pod ciśnieniem 100 barów. Typowe błędy myślowe prowadzące do takich nieprawidłowych wniosków obejmują nieprzemyślane utożsamianie ciśnienia z temperaturą, co jest częstym źródłem zamieszania. Zrozumienie wykresów fazowych oraz umiejętność ich interpretacji są kluczowe dla właściwego postrzegania zachowań substancji w różnych warunkach, co jest istotnym elementem nauk przyrodniczych i inżynieryjnych.