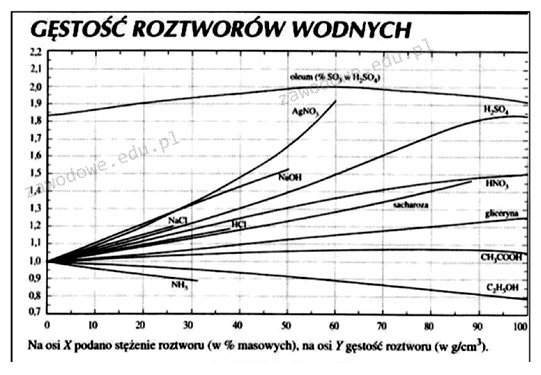
Odpowiedź 50% jest prawidłowa, ponieważ stężenie roztworu kwasu siarkowego(VI) o gęstości 1,4 g/cm³ można odczytać bezpośrednio z wykresu, który przedstawia zależność gęstości roztworów od ich stężenia. Z diagramu wynika, że dla gęstości 1,4 g/cm³ wartość stężenia wynosi około 50%. To stężenie jest istotne w kontekście różnych zastosowań przemysłowych, takich jak produkcja nawozów czy wytwarzanie chemikaliów, gdzie precyzyjne przygotowanie roztworów ma kluczowe znaczenie. Przygotowanie roztworów o określonym stężeniu jest zgodne z normami branżowymi, które wymagają dokładności i powtarzalności procesów chemicznych. Ponadto, w laboratoriach chemicznych lub przemysłowych, umiejętność odczytywania danych z wykresów oraz ich prawidłowa interpretacja jest niezbędna dla zapewnienia bezpieczeństwa oraz skuteczności przeprowadzanych reakcji chemicznych. W związku z tym, znajomość tego typu wykresów i ich aplikacji w praktyce jest kluczowa dla chemików i inżynierów chemicznych.
W przypadku stężeń kwasu siarkowego(VI) często pojawiają się błędne interpretacje wynikające z mylnych założeń dotyczących gęstości roztworów. Wybór niewłaściwego stężenia, takiego jak 55%, 45% czy 40%, sugeruje niezrozumienie podstawowych zasad dotyczących gęstości i stężenia roztworów. Przy gęstości 1,4 g/cm³, stężenia powyżej 50% są rzadko spotykane w standardowych roztworach wodnych kwasu siarkowego, a ich uzyskanie wymagałoby specyficznych warunków, które nie są typowe w większości zastosowań laboratoryjnych. Ponadto, niektóre z tych odpowiedzi mogą wynikać z typowych błędów myślowych, takich jak nieprawidłowe przeliczenia stężenia na podstawie odczytów z wykresu lub nieprzywiązywanie wagi do jednostek miary. Rozumienie zależności między gęstością a stężeniem jest kluczowe w chemii, zwłaszcza w kontekście przygotowywania roztworów. W praktyce, należy stosować się do uznawanych standardów, takich jak wytyczne dotyczące przygotowania roztworów i stosowania odpowiednich technik analitycznych, aby uniknąć błędów. Zrozumienie tych zasad pozwala na dokładniejsze i bezpieczniejsze prowadzenie badań oraz tworzenie roztworów o pożądanych właściwościach chemicznych.