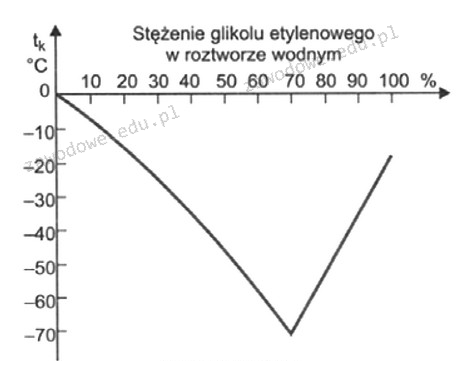
Odpowiedź 20% jest poprawna, ponieważ na podstawie wykresu, temperatura krzepnięcia roztworu wodnego z glikolem etylenowym wynosząca -15°C odpowiada stężeniu tego związku na poziomie 20%. W praktyce, stężenie glikolu etylenowego w roztworach wodnych jest kluczowe w zastosowaniu w chłodnictwie oraz w produkcji substancji przeciwzamarzających. Użycie glikolu etylenowego w odpowiednich proporcjach pozwala obniżyć temperaturę krzepnięcia wody, co jest istotne w systemach grzewczych i chłodzących. W przemyśle chemicznym, zrozumienie tego, jak stężenie wpływa na właściwości fizyczne roztworu, jest fundamentalne dla zapewnienia efektywności procesów technologicznych. Warto również zauważyć, że stężenia powyżej 20% mogą prowadzić do zwiększonego ryzyka krystalizacji, co może wpływać na wydajność całego systemu. Dlatego znajomość odpowiednich proporcji oraz ich wpływu na właściwości roztworu jest kluczowa w wielu zastosowaniach przemysłowych.
Stężenia glikolu etylenowego w roztworach wodnych mają znaczący wpływ na ich temperaturę krzepnięcia, co jest kluczowe w wielu aplikacjach przemysłowych. Wybór stężeń, takich jak 80%, 60% lub 50%, jest niewłaściwy, ponieważ prowadzi do wysoce mylnych wniosków dotyczących właściwości fizycznych roztworu. Temperatura krzepnięcia roztworu wzrasta z wyższym stężeniem glikolu etylenowego, a proporcje te są znacznie wyższe niż wartości rzeczywiste dla wskazanej temperatury krzepnięcia -15°C. Użytkownicy mogą mylnie zakładać, że wyższe stężenia glikolu zawsze skutkują niższymi temperaturami krzepnięcia, co nie jest prawdą. Typowym błędem jest również ignorowanie wykresów i danych eksperymentalnych, które jasno wskazują na konkretne wartości stężenia. Należy pamiętać, że dla osiągnięcia pożądanej temperatury krzepnięcia, kluczowe jest przestrzeganie norm i dobrych praktyk, które są oparte na badaniach naukowych i doświadczeniu inżynierów. Ustalanie odpowiednich proporcji może zapobiec problemom z krystalizacją i wydajnością systemu, co jest niezbędne dla ich długotrwałej i efektywnej pracy.