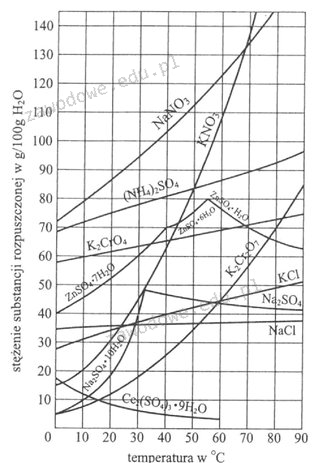
Odpowiedź 90 kg jest prawidłowa ze względu na zasady rozpuszczalności azotanu(V) potasu w wodzie, które zmieniają się w zależności od temperatury. W temperaturze 10°C rozpuszczalność tego związku wynosi około 31 g/100 ml wody, podczas gdy w temperaturze 60°C wzrasta do około 62 g/100 ml. Oznacza to, że w nasyconym roztworze w 10°C mamy w 120 kg wody maksymalnie rozpuszczone 31 kg KNO3. Aby zwiększyć stężenie do nasycenia w 60°C, musimy dodać dodatkowe ilości azotanu. Obliczając różnicę pomiędzy ilością wymaganą w 60°C a ilością istniejącą w 10°C, otrzymujemy potrzebną do dodania ilość, która wynosi 90 kg. Przykładem zastosowania tej wiedzy może być przygotowanie roztworów do celów laboratoryjnych lub przemysłowych, gdzie precyzyjne kontrolowanie stężenia substancji chemicznych jest kluczowe dla prawidłowego przebiegu reakcji chemicznych oraz uzyskiwania produktów o oczekiwanej jakości.
Wybór innych odpowiedzi często wynika z nieporozumień dotyczących pojęcia nasycenia roztworu oraz wpływu temperatury na rozpuszczalność. Odpowiedzi takie jak 20 kg lub 110 kg mogą sugerować, że respondent nie uwzględnił różnicy w rozpuszczalności azotanu potasu w dwóch różnych temperaturach. W rzeczywistości, aby określić wymaganą ilość KNO3 do dodania, należy najpierw zrozumieć, ile tego związku już znajduje się w 120 kg roztworu w temperaturze 10°C, a następnie obliczyć, ile jest potrzeba w nasyconym roztworze w 60°C. Mylne jest również stwierdzenie, że do uzyskania roztworu 60°C wystarczy dodać niewielką ilość, jak sugeruje odpowiedź 20 kg. Takie podejście ignoruje fakt, że nasycone roztwory są określane na podstawie maksymalnej ilości substancji, która może się rozpuścić w danej objętości rozpuszczalnika. Kluczowe w tym kontekście jest zrozumienie, że nasycenie jest procesem, który zmienia się w zależności od temperatury, a więc ignorowanie tej zmiany doprowadza do błędnych obliczeń. Równocześnie, dodanie 130 kg czy 110 kg KNO3 byłoby niepraktyczne, ponieważ przekraczałoby to ilość, jaką można rozpuścić w roztworze, co prowadziłoby do nadmiaru substancji i tworzenia osadu, co jest sprzeczne z definicją nasyconego roztworu. Właściwe podejście wymaga dokładnych obliczeń i zrozumienia chemii roztworów, co jest fundamentalne w chemii analitycznej i w przemyśle chemicznym.