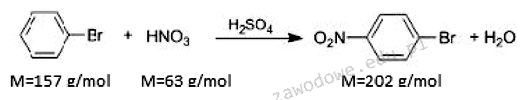
Twoja odpowiedź jest poprawna, ponieważ obliczenie masy teoretycznej stężonego HNO3 wymaga uwzględnienia zarówno stechiometrii reakcji, jak i nadmiaru technologicznego. W pierwszym kroku należało określić ilość moli bromobenzenu, co w twoim przypadku wynosi 3,14 kg / 157 g/mol = 20 moli. Następnie, według równania reakcji, do syntezy p-bromonitrobenzenu potrzebne są 20 mole HNO3. Uwzględniając 5-krotny nadmiar, otrzymujemy 100 moli HNO3. Przeliczając to na masę, uzyskujemy 100 moli x 63 g/mol = 6300 g, co odpowiada 6,30 kg HNO3. W praktyce, precyzyjne obliczenia tego typu są kluczowe w procesach chemicznych, gdzie nieodpowiednie ilości reagentów mogą prowadzić do nieefektywnych reakcji lub nawet niebezpieczeństw. W przemyśle chemicznym, przygotowanie odpowiednich ilości substancji chemicznych zgodnie z wymaganiami reakcji jest standardem, który zapewnia bezpieczeństwo i optymalizację procesów produkcyjnych.
Analizując pozostałe odpowiedzi, można zauważyć, że wiele z nich wynika z błędnych założeń dotyczących stechiometrii reakcji oraz nieprawidłowego przeliczenia mas reagentów. Na przykład, wybór odpowiedzi 15,70 kg może sugerować błędne założenie, że potrzebne jest więcej HNO3 niż to wynika z obliczeń stechiometrycznych. Tego typu pomyłki często mają swoje źródło w niewłaściwym zrozumieniu potrzebnej ilości reagentów w stosunku do ilości substratów. Z drugiej strony, wybór 1,57 kg może wynikać z błędnego przeliczenia moli lub założenia, że stosunek reagentów jest inny niż rzeczywisty. Takie podejście ignoruje zasadniczą rolę, jaką odgrywa nadmiar technologiczny. W rzeczywistości, w wielu reakcjach chemicznych, zastosowanie nadmiaru reagentu, jak w tym przypadku 5-krotnego, ma na celu zapewnienie, że reakcja zajdzie w pełni i maksymalizuje wydajność produktu. Wybór 6,30 kg jako odpowiedzi jest wynikiem precyzyjnych obliczeń, natomiast inne odpowiedzi wskazują na niedostateczne zrozumienie zasad chemicznych czy też niewłaściwe podejście do obliczeń stechiometrycznych. Dobrze jest pamiętać, że dokładność w obliczeniach chemicznych jest kluczowa dla zapewnienia efektywności i bezpieczeństwa procesów labolatoryjnych oraz przemysłowych.