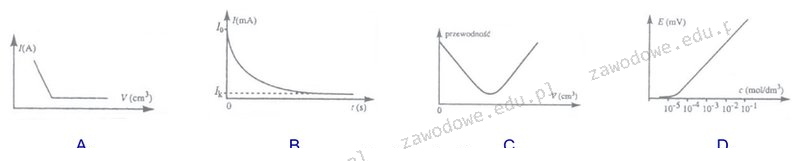
Wykres C jest prawidłowym przedstawieniem krzywej konduktometrycznej dla miareczkowania mocnego kwasu mocną zasadą ze względu na charakterystykę zmiany przewodności. W tym przypadku obserwujemy, że przewodność rośnie w miarę dodawania zasady do kwasu, osiągając punkt przegięcia, który wskazuje na punkt końcowy miareczkowania. W punkcie tym przewodność osiąga minimalną wartość, co jest typowe dla tego rodzaju reakcji chemicznych, ponieważ w momencie całkowitego zneutralizowania kwasu przez zasadę, jony przewodzące w roztworze zmieniają się. Praktyczne zastosowanie tej wiedzy znajduje się w laboratoriach chemicznych, gdzie konduktometria jest wykorzystywana do określenia stężenia roztworów oraz reakcjach miareczkowania. Standardy, takie jak ISO 7888, mówią o metodach analizy konduktometrycznej, co podkreśla znaczenie dokładnych pomiarów w chemii analitycznej.
Wybór innego wykresu może sugerować brak zrozumienia dynamiki miareczkowania konduktometrycznego. W przypadku pozostałych opcji, nie przedstawiają one typowych charakterystyk krzywych konduktometrycznych, które powinny wyraźnie ilustrować zmiany przewodności w trakcie miareczkowania. Zrozumienie, że punkt końcowy miareczkowania mocnego kwasu mocną zasadą znajduje się w miejscu, gdzie przewodność osiąga minimum, jest kluczowe. Wykresy, które nie pokazują tego przegięcia, mogą prowadzić do błędnych interpretacji związanych z równowagą chemiczną. Często spotykane błędy myślowe obejmują mylenie reakcji chemicznych o różnym charakterze, takich jak miareczkowanie kwasów słabych, gdzie zachowanie przewodności jest odmienne. Kluczowe jest, aby pamiętać, że prawidłowe zrozumienie miareczkowania wymaga nie tylko znajomości teorii, ale również praktycznych umiejętności analitycznych, takich jak umiejętność analizy wyników eksperymentalnych oraz znajomość odpowiednich standardów branżowych, takich jak metodologia opisana w dokumentach ISO dotyczących analizy chemicznej.